Oncologie : Waiv obtient le marquage CE-IVDR de deux tests de précision
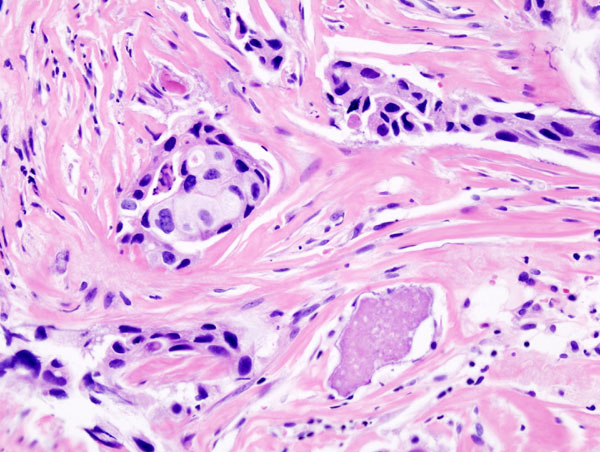
Histopathologie d'un carcinome canalaire infiltrant du sein. Biopsie à l'aiguille. Coloration à l'hématoxyline et à l'éosine.
@KGH - CC.SA 3.0
Ce marquage s’applique à deux des solutions de Waiv (ex-Owkin Dx) : RlapsRisk BC, dédié à l’évaluation du risque de rechute dans le cancer du sein et MSIntuit, utilisé pour le dépistage de l’instabilité des microsatellites (MSI) dans le cancer colorectal.
Ces deux tests sont désormais certifiés CE en conformité avec le règlement IVDR, autorisant leur déploiement clinique dans les États membres de l’Union européenne. « Il s’agit d’une étape majeure pour l’entreprise, qui renforce sa crédibilité et atteste de la fiabilité de ses solutions, dans un contexte réglementaire particulièrement exigeant, indique un communiqué de l’entreprise. Ces autorisations consolident la position de Waiv comme partenaire de confiance pour les laboratoires, les établissements de santé et les acteurs pharmaceutiques à la recherche de solutions d’IA validées. Elles marquent aussi une avancée concrète vers l’intégration de ces tests dans la pratique clinique, au bénéfice direct des patients. »
Tests de précision basés sur l’IA
RlapsRisk BC prédit le risque de récidive du cancer du sein à partir de lames d’histopathologie. Il peut fournir des informations de profilage des risques au niveau génomique à tout laboratoire d’anatomopathologie, sans examens complémentaires approfondis. En identifiant plus tôt les patients à haut risque, il doit permettre de prendre des décisions thérapeutiques plus éclairées et personnalisées. Ceci, en aidant les cliniciens à cibler les thérapies agressives lorsque cela est nécessaire et en évitant aux patients à faible risque des traitements inutiles. MSIntuit CRC, quant à lui, applique une approche de précision basée sur l’IA au cancer colorectal. Il est censé offrir un dépistage rapide et évolutif de l’instabilité microsatellitaire (MSI) à partir de lames H&E. En s’intégrant aux flux de travail de tests de routine, MSIntuit CRC identifie et exclut rapidement les patients non MSI, dans le but de rationaliser le processus de test pour l’ensemble de la population de patients. Le statut MSI est un biomarqueur essentiel pour identifier les patients susceptibles de bénéficier d’une immunothérapie ; une détection plus rapide peut accélérer l’accès à des traitements plus ciblés.
Des tests disponibles sur plusieurs plateformes
A noter que les laboratoires peuvent accéder aux tests de Waiv via Destra, une plateforme de pathologie numérique interopérable, ou en les intégrant à leurs flux de travail existants grâce à des systèmes de gestion et de visualisation compatibles, tels que Proscia, Roche Diagnostics, Sectra et Tribun Health. «L’IA va surtout agir comme un pathologiste augmenté, plus rapide, plus standardisé, capable d’exploiter énormément de données, a analysé Jean-Christophe Sabourin, président du comité d’organisation de la SFP, en guise d’introduction. Mais la responsabilité et la décision finale restent humaines. Cette journée s’inscrit comme un moment charnière pour notre discipline. L’IA n’est plus une promesse lointaine. Elle va transformer nos pratiques, nos outils, nos organisations. Elle va ouvrir des perspectives nouvelles pour la recherche, le diagnostic et la formation. »